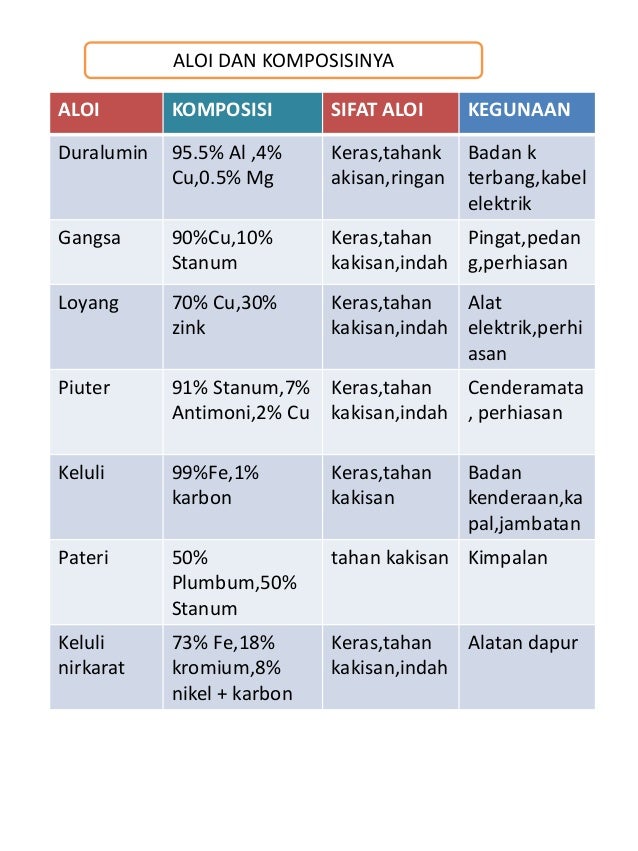
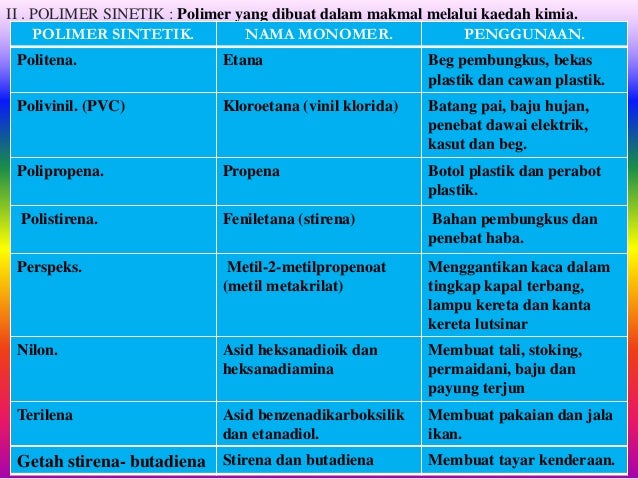
1)Memahami pembuatan asid sulfurik
Kegunaan asid sulfurik:
*penghasilan baja
*pembuatan detergen
*melembutkan kulit haiwan
Proses pembuatan asid sulfurik secara industri:
-dihasilkan melalui proses sentuh
-bahan mentah pembuatan asid sulfurik dalam proses sentuh:
=sulfur,oksigen dan air
contoh rajah pembuatan asid sulfurik melalui proses sentuh
Peringkat 1:Pembentukan sulfur dioksida
-Leburan sulfur dibakar dalam udara kering yang berlebihan untuk hasilkan gas sulfur dioksida,gas yang terbentuk ditulenkan,dikeringkan dan disejukkan.
S(ce)+O₂(g)=SO₂(g)
Peringkat 2:Pembentukan gas sulfur trioksida
-Sulfur dioksida dan gas oksigen yang berlebihan disalurkan melalui mangkin vanadium (V) oksida pada suhu 450°C dan tekanan 1 atm untuk menghasilkan sulfur trioksida
-Sulfur dioksida dan gas oksigen yang berlebihan disalurkan melalui mangkin vanadium (V) oksida pada suhu 450°C dan tekanan 1 atm untuk menghasilkan sulfur trioksida
2SO₂(g)+0₂(g)=2SO₃(g)
-Kira-kira 99.5 peratus gas sulfur trioksida dapat dihasilkan melalui tindak balas berbalik yang eksotermik
Peringkat 3:Pembentukan oleum
-Sulfur trioksida dilarutkan dalam asid sulfurik pekat untuk membentuk oleum
SO₃(g)+H₂SO₄(ce)=H₂S₂O₇(ce)
Peringkat 4:Pencairan oleum
-Oleum dicairkan dengan air untuk hasilkan asid sulfurik pekat dalam kuantiti yang banyak
H₂S₂O₇(ce)+H₂O(ce)=2H₂SO₂(ce)
Sulfur trioksida tidak dilarutkan secara langsung ke dalam air untuk hasilkan asid sulfurik
S0₃(g)+H₂0(ce)=H₂SO₄(ce)
Sulfur dioksida dan pencemaran alam sekitar
Punca:
- pembakaran sulfur dalam proses sentuh
- pengekstrakan logam dari bijih sulfida
- pembakaran bahan api fosil (petroleum,gas asli,arang batu)
- mengakis bangunan dan arca yang diperbuat daripada marmar atau batu kapur
- mengurangkan nilai pH dalam tanah
- meningkatkan keasidan air dalam tasik dan sungai
- ammonia atau ammonium hidrosida untuk hasilkan ammonium sulfat
- kalsium hidroksida atau kalsium karbonat untuk hasilkan kalsium sulfat